|
&more
 >
Chemische Energiespeicherung
>
Chemische Energiespeicherung
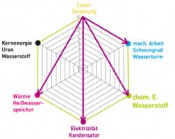
Chemische EnergiespeicherungAbgesehen von der Geothermie und den Gezeiten ist unser Heimatstern die einzige nachhaltige primäre Energiequelle, die uns noch Jahrmillionen zur Verfügung steht. Alle nachhaltigen Energieversorgungssysteme müssen daher zwingend direkt von der Sonne ausgehen. Ihre Strahlungsenergie ist 100 Prozent Freie Enthalpie (Exergie) und kann direkt in alle anderen Energieformen (Kernenergie ausgenommen) umgewandelt werden (Abb. 1). Daher ist es eine wichtige Zukunftsaufgabe, die auf die Erde einfallende Sonnenstrahlung über wirkungsgradoptimierte Wandlungsketten in nutzbare Energieformen, wie z.B. Elektrizität oder Wasserstoff, umzuwandeln. Der heute universellste Energieträger ist elektrischer Strom, der nach dem Stand der Technik via Fotovoltaik, Solarthermie, Wind- und Wasserkraft aus der Sonnenstrahlung erzeugt werden kann; nachteilig ist seine begrenzte Speicherbarkeit, was die deutsche Energiewende vor ernste Probleme stellt. Die Energiedichte der heutigen Akkumulatoren (z.B. Li-Ionen-Akku mit bis zu ca. 0,3kWh kg-1) sind für Fahrzeuge nur begrenzt ausreichend, von Flugzeugen ganz zu schweigen. Daher ist es sinnvoll, elektrische Energie in chemischen Bindungen zu speichern, um deren hohe Energiespeicherkapazität zu nutzen.
Abb. 1 Unser „Energienetz“: Die sechs bekannten Energieformen und Beispiele für ihre direkten Speichermöglichkeiten. Die Sonnenstrahlung kann ohne Umwege in alle anderen Energieformen umgewandelt werden, die Kernenergie ausgenommen.
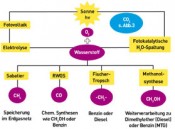
Abb. 2 Wandlungsketten, um aus Sonnenstrahlung über Solar-H2 und CO2 Kohlenwasserstoffe aufzubauen.
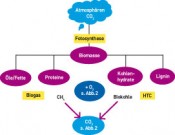
Abb. 3 Isolierung des Atmosphären-CO2 (ca. 400 ppm (v/v)) über Biomasse via Biogasanlagen bzw. Anlagen zur hydrothermalen Carbonisierung (HTC-Anlagen) zu reinem CO2.
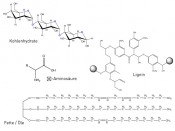
Abb. 4 Strukturbeispiele der vier mengenmäßig bedeutendsten Biomasse-Bestandteile: Kohlenhydrate (Beispiel einer Teilstruktur von Stärke), Lignin (Beispiel einer Teilstruktur), Fette/Öle (Beispiel eines Triglycerids mit Linol-, Stearin- und Ölsäure).
Als chemischer Energieträger kommt vor allem Solar-Wasserstoff, hergestellt via Wasserelektrolyse (Stand der Technik) oder fotokatalytischer H2O-Spaltung (Stand der Forschung) in Frage (Abb. 2). Wasserstoff ist aber ähnlich wie Strom schlecht speicherbar und birgt ein nicht zu unterschätzendes Gefahrenpotenzial. Einen Ausweg aus dem Dilemma ist es, den Wasserstoff in den C-H-Bindungen von Kohlenwasserstoffen zu speichern, wie z.B. CH4, -CH2-, CH3OH u.a. Die Kohlenwasserstoff-Form mit der besten Speicherbarkeit, der höchsten Speicherdichte, der dichtesten Infrastruktur sowie dem geringsten Sicherheitsrisiko ist Dieselkraftstoff. Das Standarddiesel-Molekül ist n-Hexadekan (Cetan). Es ist mit einem Flammpunkt von 135°C nicht brennbar im Sinne des Gefahrstoffrechts; die Infrastruktur und Logistik ist weltweit etabliert. Daher ist es ein sinnvolles Zukunftskonzept Solar-Wasserstoff mit Kohlendioxid in Methan, Dieselkraftstoff (= -CH2-) oder Methanol via: Sabatier CO2 + 4 H2 -> CH4 + 2 H2O(g) , Δ RH0 = -166kJ mol-1 Fischer-Tropsch CO2 + 3 H2 -> -CH2-(g) + 2 H2O(g) , Δ RH0= -117kJ mol-1 Methanol CO2 + 3 H2 -> CH3OH(g) + H2O(g) , Δ RH0 = -50kJ mol-1 umzuwandeln bzw. zu speichern (Abb. 2). Das dafür benötigte CO2 kann heute und für die mittlere Zukunft effektiv aus den Rauchgasen von Kohlekraftwerken mit etablierten Technologien isoliert werden. Nachhaltig ist jedoch nur die Isolierung des Atmosphären-CO2 – eine hohe technische Herausforderung – da eine Isolierung via Ad- bzw. Absorption schon aufgrund der geringen Konzentration (400ppm (v/v) auf 99Vol.-%, d.h. Anreicherungsfaktoren bis 2500) und der Staubbelastung der Luft unrealistisch ist; unsere Luft enthält massenmäßig mehr Staub als CO2. Bleibt nur, mit Hilfe der grünen Pflanzen via Fotosynthese das CO2 aus der Atmosphäre zu isolieren (Abb. 3): CO2 + H2O(l) -> -C(H2O)- + O2 , Δ RH0 = +466kJ mol-1 Diese speichern es überwiegend in Form von Kohlenhydraten (-C(H2O)-). Daraus kann mit Hilfe der anaeroben Fermentation (Biogas, etabliert) oder der chemischen Dehydratisierung durch hydrothermale Carbonisierung, HTC abgekürzt (Biokohle, Pilotierung) reines CO2 gewonnen werden, wenn man die Produkte Methan bzw. Kohle mit dem bei der H2O-Elektrolyse freigewordenen Sauerstoff verbrennt (Abb. 3): Biogas-Herstellung und Verbrennung mit Elektrolyse-Sauerstoff 2 -C(H2O)– -> CO2 + CH4 , Δ RH0 = -45kJ mol-1 CH4 + 2 O2 -> CO2 + 2 H2O(g) , Δ RH0 = -802kJ mol-1 Biokohle-Herstellung und Verbrennung mit Elektrolyse-Sauerstoff -C(H2O)- -> C + H2O , Δ RH0 = -73 kJ mol-1 C + O2 -> CO2 , Δ RH0 = -393kJ mol-1 Ein Problem beim Einsatz der beiden Technologien ist, dass keine für sich genommen die Bestandteile der Biomasse optimal verwerten kann. Von den vier großen Stoffgruppen, aus denen Biomasse besteht (s. Abb. 4), wird von Biogasanlagen die Lignin-Fraktion praktisch nicht verwertet; von Biokohleanlagen werden Fette/Öle sowie die Proteinfraktion kaum verkohlt. Nur eine Kombination beider Technologien kann alle Stoffgruppen vollständig in die gewünschten Zwischenprodukte Biogas und Biokohle umwandeln, deren Verbrennung mit dem reinen Sauerstoff der Wasserelektrolyse das gewünschte reine CO2 liefern.
Damit stehen die Synthesebausteine für Solarfuels, nämlich CO2 und Solar-H2, nachhaltig für die in Abb. 2 aufgeführten Synthesen von Kohlenwasserstoffen (CH4, -CH2-) und Oxigenaten wie CH3OH zur Verfügung: CO2 + 4 H2 -> CH4 + 2 H2O(g) , Δ RH0 = -166 kJ mol-1 Die Umsetzung von CO2 mit H2 via heterogen katalysierter Gasphasenreaktionen nach Fischer-Tropsch mit vorgelagerter Revers-Wassergas-Shift-Reaktion (RWGS) ist Stand des Wissens bzw. der Technik; nachteilig ist hierbei die hohe Investition. Durch neue Forschungsansätze soll dieser Nachteil überwunden werden, damit CO2 und H2 einstufig zu Kohlenwasserstoffen umgesetzt werden können. CO2 + H2 -> CO + H2O(g) , Δ RH0 = +41kJ mol-1 CO + 2 H2 -> -CH2-(g) + H2O(g) , Δ RH0 = -157kJ mol-1 Methanol, ein idealer Otto-Kraftstoff, kann durch Gasphasendehydratisierung an sauren Zeolithen in Dimethylether, einem idealen Diesel-Kraftstoff, überführt werden. Dieser wiederum kann durch Zeolithkatalysatoren in verschiedene Kohlenwasserstoffe umgewandelt werden (Methanol-to-Olefins, Methanol-to-Aromatics, Methanol-to-Gasoline). CO2 + 3 H2 -> CH3OH(g) + H2O(g) , Δ RH0 = -50kJ mol-1 2 CH3OH(g) > CH3OCH3 + H2O(g) , Δ RH0 = -24kJ mol-1 CH3OH(g) -> -CH2-(g) + H2O(g) , Δ RH0 = -67kJ mol-1 Damit kann via Verbrennung der so gewonnenen Solarfuels im Motor oder Kraftwerk die Energie der Sonne indirekt über das Speichermedium Kohlenwasserstoffe für unsere transiente Mobilität (Tag/Nacht) und unseren Wärmebedarf (Sommer/Winter) nachhaltig genutzt werden. Foto ©: NASA |
C&M 4 / 2013
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:Weitere Artikel online lesenNewsAhlborn GmbH: Hochgenaue Temperaturmessung mit digitalen FühlernBei über 80 % aller industriellen Messaufgaben werden Temperaturen gemessen. Wichtig ist das Zusammenspiel von Messgerät und Fühler sowie die verwendete Technologie. Aus der Präzisionsschmiede, der Firma Ahlborn aus Holzkirchen bei München, kommt jetzt ein Messsystem für hochgenaue Temperaturmessung, das nicht nur im Labor verwendet werden kann.© Ahlborn Mess- und Regelungstechnik GmbH |
Suche: